Knoglevæv kaldes også benvæv og er specialiseret tæt bindevæv. Det forener stor hårdhed og styrke med mindst mulig vægt. Det fungerer som støtteorgan, er et led i calciumhomeostasen og beskytter.
Makroskopisk struktur
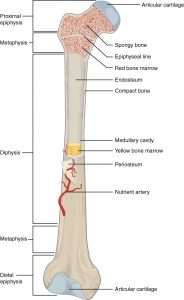
Skaftet på en knogle kaldes diafysen og består af kompakt knoglevæv der som rør omgiver knoglemarven. Enderne kaldes epifysen og består stort set udelukkende af spongiøst knoglevæv der yderst går over i et tyndt lag kompakt knoglevæv. Overgangen mellem diafyse og epifyse kaldes metafysen. Ledfladerne er beklædt med hyalin brusk (ledbrusk). Resten af knoglen er beklædt med en benhinde kaldet periost der er tæt bindevæv. Marvhulen og hulrum i spongiøst knoglevæv er beklædt med en tynd hinde af cellerigt bindevæv kaldet endost. Diffusion i knoglematrix er ikke muligt pga. forkalkning af denne.
Knoglevævstyper
Der findes to typer knoglevæv: Spongiøst knoglevæv og Kompakt knoglevæv. De fleste knogler består af begge typer, dog i meget varierende mængde.
Spongiøst knoglevæv
Spongiøst knoglevæv kaldes også substantia spongiosa eller en trabekulær knogle. Består af fine bjælker eller plader (trabeculae), der danner svampeagtigt netværk. Det kommunikerende hulrum er udfyldt af knoglemarv.
Spongiøst knoglevæv består af intercellulær substans knoglematrix der danner lameller. Haverske kanaler og Volkmannske kanaler findes ikke – det spongiøse knoglevæv er avaskulært.
Vævet er opbygget af trabekulære osteosoner der er en flad skive (60 µm tyk og 600 µm lang). Den er opbygget af 20 lameller løbende parallelt med skivens flade.
Trabekler er sammensat af én til flere trabekulære osteosoner med mellemliggende cementlinier og når en tykkelse på 50-400 µm. Specielt i knoglevæv som belastes er trabeklerne tykkest i belastningens retning. Disse afstives af tyndere, tværgående trabekler.
Spongiøst knoglevæv udgør kun 20% af totalt knoglemasse, men står for hele 80% af den metaboliske aktivitet. Derfor er spongiøst knoglevæv også mere følsom overfor knogletab, da det oftere udskiftes. Det er også derfor det er i spongiøst knoglevæv at man ser det første tab af knoglemasse ved postmenopausal osteoporose.
Kompakt knoglevæv
Kompakt knoglevæv kaldes også substantia compacta eller en cortikal knogle. Består af kompakt masse uden synlige hulrum.
Kompakt knoglevæv består af intercellulær substans kaldet knoglematrix der danner 3 µm tykke lag kaldet lameller. Knoglecellerne osteocytterne ligger i små hulrum kaldet laguner i lamellerne.
Lamellerne er arrangeret koncentrisk omkring længdeforløbende Haverske kanaler hvorved de Haverske systemer/Cortikale osteoner dannes. En Haversk kanal er 50 µm i diameter og indeholder 1-2 kapillærer, nervetråde og bindevæv. Et haversk system indeholder ca. 15 lameller og er 150 µm i diameter og 3 mm lang. Ses i tværsnit som ringe omkring kanalen. En lamel består overvejende af parallelt forløbende kollagene fibre type I og fiberretningen skifter fra lamel til lamel.
Rester af nedbrudt haverske systemer fra remodellering kaldes interstitielle lameller.
Kompakt knoglevæv udgør hele 80% af den totale knoglemasse, men står kun for 20% af den metaboliske aktivitet.
Knoglematrix
Er en extracellulær matrix der består af organisk matrix og uorganiske salte. Den organiske matrix består af kollagene fibre type I indlejret i grundsubstans der består af proteoglykaner og andre små molekyler. Den uorganiske matrix består af udgør 75% af tørvægten hos voksne og består af krystallinsk form af calcium-phosphat kaldet hydroxyappatit og andre ioner.
Mineralisering
Mineralisering kaldes også for calcifikation og er betegnelsen for deponering af mineraler i den organiske matrix i brusk og knoglevæv. Herved sker der udfældning af calcium- og phosphationer der omdannes til hydroxyappatit.
Epifyseskive
Under længdevæksten af rørknogler dannes en epifyseskive, der ved længdevækstens afslutning mineraliseres til en epifyselinie.
Peak bone mass
Overvægt af knogledannelse fører til øget knoglemasse indtil maximum nås, kaldet peak bone mass.
Mikroskopisk struktur
Knogler består af såvel cellulære som ikke-cellulære komponenter. Den indre og ydre overflade af knogler er dækket af henholdsvis endost og periost. Disse er fibrøse membraner, som er fyldt med osteogene celler organiseret lagvis. I endost og periost er de knogledannende celler, osteoblaster, og de knogleresorberende celler, osteoklaster, beliggende. Dybt i knoglen ligger osteocytter indlejret i lakuner med lange processer rige på mikrofilamenter, og er forbundet med gap junctions til andre osteocytter samt til osteoblaster og osteoklaster på knogleoverfladen. Disse processer ligger i snævre kanalikuli, der penetrerer knoglevævet som et fintmasket net. Rundt om processerne er det periosteocytiske rum, som er fyldt med en ekstracellulærvæske med en [Ca2+] på 1.0 mM, i modsætningen til plasmas [Ca2+], som er 1.5 mM.
De ikke-cellulære komponenter af knoglevævet er kollagen fibre. Disse er primært kollagen type 1 og udgør 90 % af den totale proteinmængde i knogler. Kollagenfibrene er arrangeret i en
lamelstruktur. Der er også non-kollagen proteiner, som omfatter komponenter af grundsubstansen (glykoproteiner og proteoglykaner), vækstfaktorer m.v. Endelig er mineralerne en vigtig del af knoglen, idet det er disse, som giver knoglerne deres hårde egenskaber. Calcium er primært oplagret i knogler som hydroxyapatit krystaller, som er bundet til kollagenfibrene.
Knoglens celler
Knoglens celler hedder osteocytter. Herudover er der 4 andre celletyper kaldet osteoblaster, osteoklaster, Osteprogenitorceller og Lining cells.
Osteocytter
Osteocytter er den egentlige knoglecelle. Opstår fra osteoblaster. Kommunikerer med hinanden og lining cells via gap junctions. Ernæres via den interstitielle vævsvæsle i canaliculi.
De ligger i små hulrum i knoglerne kaldet laguner. Osteocytterne har mange spinkle udløbere der løber i fine kanaler kaldet Canaliculi. Canaliculi afgår vinkelret på lakunerne og anastomoserer med hinanden og karholdige kanaler i knoglevævet samt den indre og ydre overflade. Herved kan tilføres og afgives substanser via den sparsomme mængde vævsvæske der omgiver udløberne i canaliculi.
Ernæringen af osteocytterne sker ved diffusion fra den endostale overflade via de kommunikerende canaliculi.
Osteoprogenitorceller
Udvikles fra mesenchymceller. Forekommer i fostrets mesenchym nær ossifikationscentre og senere i knoglemarv, endost og det dybe lag af periost. Har ovale, lyse kerner og uregelmæssigt, afgrænset, lyst cytoplasma (ligner fibroblaster). Kan differentiere og udvikles til osteoblaster (stamceller).
Osteoblaster
Osteoblaster er de celler, der er ansvarlige for knogleformationen. De stammer fra mesenkymale multipotente stamceller, som residerer i knoglemarven. Disse multipotente celler er selvfornyende og højproliferative, og på særlige stimuli kan de differentiere til enten celler af osteoblastlinien eller til myocytter, adipocytter eller fibroblaster. Osteoblastcellelinien omfatter:
- osteoprogenitorceller
- præosteoblaster
- osteoblaster
- lining cells
- osteocytter
Modne osteoblaster har kubisk form og er beliggende lagvis. Deres aktivitet er velkoordineret, og de producerer den lamellære knoglestruktur ved at secernere knoglematrix og efterfølgende
mineralisere denne ved hjælp af alkalisk fosfatase.
Osteoblasterne er endvidere ansvarlige for produktionen af en lang række andre proteiner involveret i knoglenydannelsen såsom det i knoglematrix vigtigste protein kollagen type 1, samt mange ikke-kollagen proteiner såsom osteopontin, osteonectin, knogle sialoprotein, biglycaner, decorin, osteocalcin, samt receptor aktivator af nuklear faktor-kappa-B ligand (RANKL) og osteoprotegerin (OPG), hvor RANKL og OPG er betydende for dannelsen og reguleringen af osteoklastdannelsen og osteoklastaktiviteten, og osteocalcin formentlig, udover regulation af knogleomsætningen, også er involveret i regulation af organismens energiomsætning. Osteoblaster kan danne ca. 0.5 µM matrix pr. dag og den formative del af knogleremodeleringscyklus tager ca. 90 dage, dog med store variationer.
Under remodeleringsprocessen bliver en del af osteoblasterne indlejret i den mineraliserede matrix og omdannes til osteocytter, mens andre bliver udfladede celler, som dækker den hvilende
knogleoverflade, også kaldet lining cells. Osteocytterne er de celler, der forekommer i størst antal i knoglerne, og danner et udstrakt netværk gennem såvel trabekulær som kompakt knogle.
Osteoblaster responderer på mange knogleaktive substanser, hormoner og vækstfaktorer, hvoraf nogle er resorptive stimuli. D-vitamin, parathyreoideahormon (PTH), glukokortikoider,
prostaglandin E2, interleukin-1 (IL-1), tumor nekrosis faktor alfa (TNF-alfa), lipopolysakkarider, østrogen, vækstfaktorer, bone morphogenetic proteins (BMP) og en lang række andre faktorer virker via osteoblaster, hvilket bekræfter osteoblasternes rolle som hovedregulator af knogleomsætningen.
Lining cells
Lining cells kaldes også knoglebeklædende celler eller overfladeosteocytter. Opstår fra osteoblaster efter afsluttet knogledannelse. Beklæder alle indvendige og udvendige knogleoverflader, hvor der ikke er aktivitet af osteoblaster eller osteoklaster. Hviler på tyndt lag osteoid. Kan efter aktivering secernere kollagenase hvilket fører til at osteoid nedbrydes hvilket fører til at lining cells viger pladsen for osteoklaster.
Osteoklaster
Osteoklaster er den knoglenedbrydende celle. Det er multinukleære kæmpeceller (100 µm) med 5-10 kerner (under patologiske forhold op til 200 kerner/celle). Cytoplasmaet er typisk acidofilt. De er lokaliseret i Howshipske lakuner – men er aktivt bevægelige. Under knoglenedbrydning fagocyterer osteoklaster rester af osteocytter, kollagen og mineral.
Knogleresorption starter oftest efter aktivering af osteoklasterne med signaler fra osteoblaster/lining cells. Biologien af disse signaler er endnu ikke komplet belyst, men RANKL og makrofag kolonistimulerende faktor (M-CSF) er nøglefaktorer, som er ansvarlige for differentiering af forstadier til modne osteoklaster. Omvendt reguleres effekten af RANKL af OPG, som er en solubel cytokinreceptor, som virker som en decoyreceptor for RANKL, og dermed blokerer for effekten af denne.
Disse medfører, at forstadier fusionerer og adhærerer til knogleoverfladerne. Vitronektin, som er et integrin, binder osteoklaster tæt til knoglen via en celle-matrix interaktion, og der skabes en nærmest forseglet spalte mellem osteoklastens ruffled border og knogleoverfladen. Ved hjælp af protonpumper pumpes syre ind i denne spalte, hvilket fører til opløsning af calciumkrystallerne i knogleoverfladen. Herefter er knoglematrix tilgængelig for nedbrydning via de store mængder lysosomale enzymer, som osteoklasten har oplagret i vesikler i cytoplasmaet. Knoglenedbrydningen resulterer I dannelsen af den såkaldte resorptionspit. På et givent signal fra osteoblaster stopper osteoklastaktiviteten og osteoklasterne migrerer til andre steder, hvor knogleresorption skal foregå, eller de undergår apoptose.
Funktioner
Skelettet er det overordnede organ for calciumhomeostasen og desuden et betydeligt lager for andre mineraler, såsom phosphat, magnesium, kalium og bikarbonat. Knogler yder mekanisk støtte for de bløde væv og fungerer som vægtstang for musklerne. Ydermere bliver de livsvigtige organer beskyttet af skelettet: ribbenene beskytter hjerte og lunger, kraniet beskytter centralnervesystemet og knoglecortex på de lange rørknogler beskytter knoglemarven, som hos voksne er det mest betydende hæmatopoietiske organ.
Funktionerne af knoglevæv er altså:
- Calciumhomeostase
- Lager for mineraler
- Mekanisk støtte for blød væv
- Vægtstang for muskler
- Beskyttelse af livsvigtige organer
Knoglemarven er et vigtig hæmatopoietiske organ. Reguleringen af knogleomsætningen er en kompleks og meget nøje reguleret proces. Den er et resultat af de knogledannende (knogleformation) og knoglenedbrydende (knogleresorption) processer. Knogleformation og knogleresorption udføres af specialiserede knogleceller, henholdsvis osteoblaster og osteoklaster. Disse to processer er tæt koblet, og er under normale omstændigheder reguleret således, at knoglemassen vedligeholdes og holdes konstant for at modstå frakturer.
En række faktorer regulerer remodelleringen af skelettet. Systemiske hormonelle faktorer virker på knoglecellerne, både direkte og indirekte, hvor de modulerer receptorekspression, receptoraktivering,
syntese eller receptorbinding af lokale faktorer. Dette resulterer i enten en øget eller nedsat knogleformation eller knogleresorption. Disse lokale faktorer, såsom cytokiner, vækstfaktorer og
prostaglandiner, kan omvendt regulere følsomheden af knoglecellerne overfor hormonelle faktorer ligesom de kan regulere aktiviteten af knoglecellerne selv.
Knogleremodellering
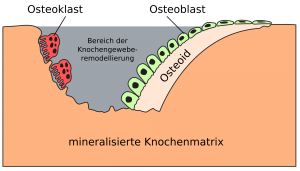
Skelettet er et dynamisk organ, som kontinuerligt bliver omsat. Der foregår således til stadighed både knogleresorption og knogleformation i en proces, som kaldes knogleremodellering. De celler, som er ansvarlige for knogleresorptionen og knogleformation er henholdsvis osteoklaster og osteoblaster. Aktiviteten af osteoblaster og osteoklaster er koblede. Primitiv, ikke-laminært knoglevæv udskiftes med modent, laminært knoglevæv. Formålet er at forny gammel knoglevæv og opretholde calciumhomeostasen.
Der foregår en konstant omsætning af knoglevævet for at regulere kalcium og andre mineraler med cirkulationen, idet knoglerne er kroppens største buffer og lager af mineraler. Knogleremodeleringen foregår konstant i det regenererende skelet på multiple steder. Det enkelte remodeleringssted kaldes en basal multicellulær enhed (BMU).
Mononukleære osteoklastforstadier bliver induceret til at fusionere og danne osteoklaster som respons på signaler fra osteoblaster. De migrerer derefter til knogleoverflader, og begynder at resorbere knogle. Den aktive resorptionsperiode er oftest ca. 3 uger, og som respons på signaler, som endnu ikke er kendt i detaljer, stopper de knogleresorptionen og migrerer derefter til andre BMU eller undergår apoptose og dør. Osteoblaster invaderer derefter resorptionskaviteten og begynder at fylde denne op med umineraliseret matrix, også kaldet osteoid.
Derefter mineraliserer de matrix for dermed at danne mineraliseret knogle. Hos raske voksne tager knogleformationsprocessen tre til fire måneder. Hos yngre raske vil den dannede mængde knogle
modsvare den resorberede mængde, men hvis formationen er inkomplet, vil der opstå et netto knogletab i hver remodeleringscyklus, som med tiden vil føre til et klinisk betydende knogletab og
dermed osteoporose.
En række faktorer har indflydelse på balancen mellem knogleformation og knogleresorption. Mange parakrine og autokrine faktorer influerer balancen mellem de to processer, herunder PTH, vitamin D, calcitonin, insulin, væksthormon, kønshormoner, glukokortikoider, thyreoideahormoner, cytokiner ((IL-1, TNF-alfa, interleukin-6), vækstfaktorer og RANKL-systemet, ligesom fysisk påvirkning af knoglerne og de deri involverede systemer.
Ossifikation
Man skelner mellem intramembranøs ossifikation og endochondral ossifikation når man taler om udvikling af knoglen.
Intramembranøs ossifikation
Udvikling af knoglen direkte i det primitive mesenchym.
Knogledannelsen begynder i mesenchymet. Mesenchymcellerne deler sig og kondenseres. Differentierer til osteoblaster, der secernerer organisk knoglematrix. Denne – endnu uforkalkede – matrix benævnes Osteoid (En tæt, homogen, eosinofil masse).
Knoglematrix mineraliseres – bliver mere eosinofil (altid en zone af svagere farvet osteoid imellem osteoblasterne og den forkalkede knoglematrix).
Yderligere matrix deponering – osteoblaster indlejres og omdannes til osteocytter
De flade kranieknogler, mandibula og clavicula er dannet på denne måde.
Endochondral ossifikation
Udvikling af knoglen finder sted i anlagt bruskmodel (indirekte). Langt de fleste knogler udvikles på denne måde.
Lavet ud fra model af embryonal, hyalin brusk omgivet af perichondrium. I midten af det fremtidige knogleskaft dannes det primære (diafyseale) ossifikationscentrum.
Chondrocytter hypertrofierer hvilket fører til at lakunerne vokser hvilket fører til at bruskmatrix reduceres til tynde septa og calcifikation af disse septa (mere basofile) hvilket fører til at chondrocytter degenererer og dør (apoptose).
Samtidig vil cellerne i perichondriet (periost) omkring skaftmidten få osteogenetiske egenskaber hvilket fører til at de differentierer til osteoprogenitorceller hvilket bliver til osteoblaster hvilket fører til dannelse af et tyndt lag knoglevæv omkring skaftmidten – periostale manchet og herigennem (indvæksttap) vokser vaskulariseret bindevæv fra periost ind og fylder hulrummene i bruskmatrix.
Gennem indvæksttappen kommer også mesenchym-celler, der differentierer til primitiv knoglemarv og osteoblaster – disse sætter sig på brusktrabeklerne (basofile) og aflejrer knoglematrix (eosinofilt) – udenpå ligger lag af osteoblaster.
Sidst opdateret 19. maj 2023
